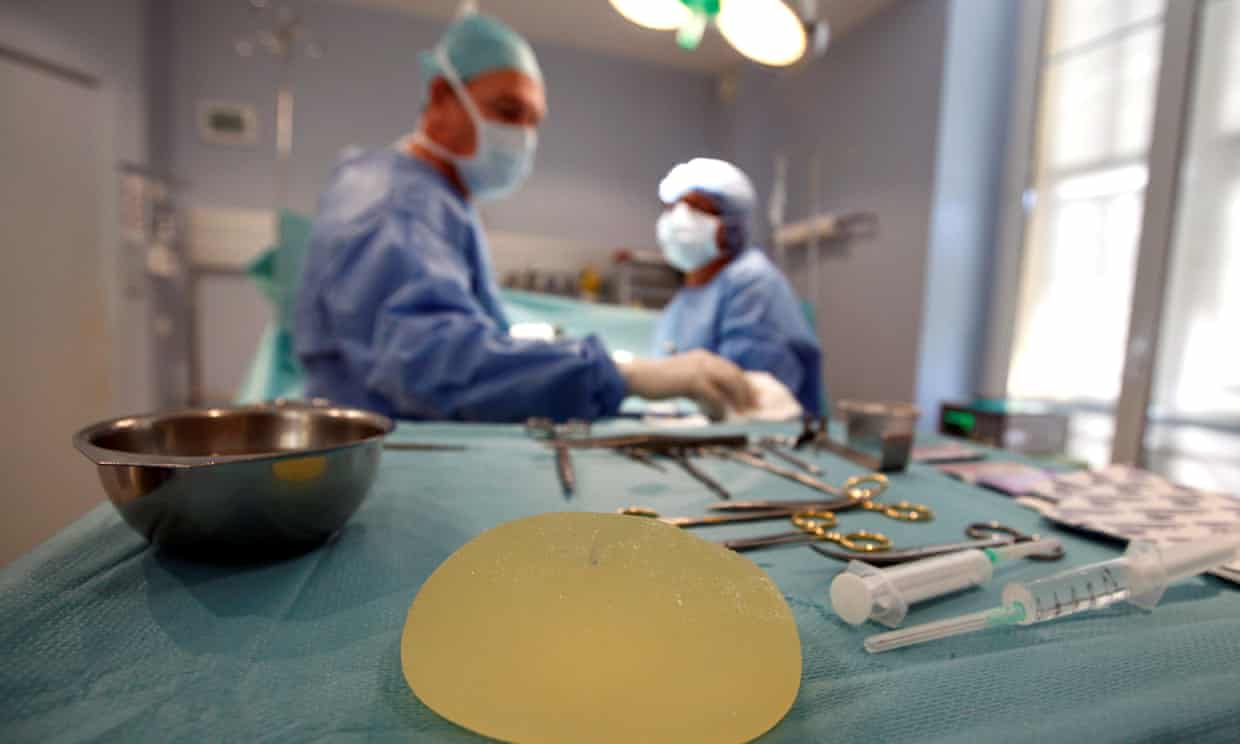
Οι δικηγόροι ζητούν αυστηρότερες προειδοποιήσεις για τα εμφυτεύματα στήθους, καθώς κυβερνητικά στοιχεία δείχνουν ότι τουλάχιστον 88 γυναίκες στο Ηνωμένο Βασίλειο έχουν διαγνωστεί με καρκίνο που συνδέεται με την επέμβαση.
Ένας μικρός αριθμός γυναικών που έχουν εμφυτεύματα μπορεί να αναπτύξει έναν σπάνιο τύπο λεμφώματος γνωστό ως “Breast Implant Associated Anaplastic Large Cell Lemphoma” (BIA-ALCL).
Αρκετοί τύποι εμφυτευμάτων που συνδέονται συχνότερα με τη νόσο – γνωστά ως εμφυτεύματα με υφή – απαγορεύονται στη Γαλλία και την Αυστραλία.
Ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ εξέδωσε προειδοποιήσεις για το «μαύρο κουτί» – τις πιο αυστηρές προειδοποιήσεις για φάρμακα και ιατρικές συσκευές – τον Οκτώβριο για τα εμφυτεύματα στήθους, συμπεριλαμβανομένης της συσχέτισής τους με το BIA-ALCL.
Έχουν αναφερθεί 733 περιπτώσεις αυτού του καρκίνου που συνδέονται με εμφυτεύματα στήθους παγκοσμίως και 36 θάνατοι.
Ο Ρυθμιστικός Οργανισμός Φαρμάκων και Προϊόντων Υγείας του Ηνωμένου Βασιλείου (MHRA) παρείχε στον Observer τον αριθμό 88 αναφορών επιβεβαιωμένων κρουσμάτων BIA-ALCL σε ασθενείς στο Ηνωμένο Βασίλειο έως τις 31 Οκτωβρίου.
Αυτό περιλαμβάνει ορισμένες περιπτώσεις, όπου η αρχική επιχείρηση δεν ήταν στη Βρετανία.
Ο κλάδος της αισθητικής χειρουργικής υποβλήθηκε σε αυστηρότερο ρυθμιστικό έλεγχο το 2010, αφού διαπιστώθηκε ότι τα εμφυτεύματα στήθους που κατασκευάζονται από τη Γαλλική εταιρεία Poly Implant Prothèse (Pip) είχαν γεμίσει με φθηνή βιομηχανική σιλικόνη μη εγκεκριμένη για ανθρώπινη χρήση.
Υπολογίστηκε ότι περίπου 50.000 Βρετανίδες είχαν τοποθετήσει εμφυτεύματα Pip, τα οποία είχαν υπερδιπλάσια συχνότητα ρήξης από άλλα εμφυτεύματα.
Στη συνέχεια δημιουργήθηκε μητρώο εμφυτευμάτων μαστού , αλλά δεν είναι υποχρεωτικό και χιλιάδες γυναίκες λείπουν από αυτό.
Η Carole Roberts, 61 ετών, από το Derby, έβαλε εμφυτεύματα Pip σε ιδιωτική κλινική του Λονδίνου το 2004.
Αφαιρέθηκαν μετά την εμφάνιση του σκανδάλου και αντικαταστάθηκαν με εμφυτεύματα υφής σε ιδιωτικό νοσοκομείο στο Μπέρμιγχαμ το 2012.
Επτά χρόνια αργότερα, διαγνώστηκε με BIA -ΑΛΚΛ.
Η Carole Roberts, είπε: «Ανησυχούσα γιατί βρήκα ένα εξόγκωμα κάτω από το μπράτσο μου. Διαγνώστηκα με BIA-ALCL και οι γιατροί μου είπαν ότι «αυτό δεν είναι καρκίνος του μαστού, αυτό εξαρτάται από τα εμφυτεύματα σας».
Ήμουν σε απόλυτο σοκ.
Δεν μου είχαν δοθεί καμία προειδοποίηση για τους κινδύνους».
Η Ρόμπερτς ανάρρωσε μετά από επέμβαση αφαίρεσης των εμφυτευμάτων, ακολουθούμενη από χημειοθεραπεία και ακτινοθεραπεία.

Είναι τώρα μία από τις οκτώ γυναίκες που εκπροσωπούνται από τη νομική εταιρεία Leigh Day που διαγνώστηκαν με BIA-ALCL, και σχεδιάζουν νομικές ενέργειες για τις υποτιθέμενες αστοχίες του προϊόντος των εμφυτευμάτων τους.
Η Bozena Michalowska Howells, επικεφαλής της νομοθεσίας για την ασφάλεια προϊόντων και τους καταναλωτές στο Leigh Day, είπε ότι οι ασθενείς πρέπει να είναι καλύτερα ενημερωμένοι για τον κίνδυνο.
Όπως επισήμανε: «Θα πρέπει να υπάρχουν καλύτερες προειδοποιήσεις και πιο στενή παρακολούθηση.
Το μητρώο εμφυτευμάτων στήθους πρέπει επίσης να είναι υποχρεωτικό.»
Η Sarah Moore, συνεργάτης στη νομική εταιρεία Hausfeld, η οποία έχει εργαστεί για την ευθύνη προϊόντων που αφορούν ιατρικές συσκευές, τόνισε:
«Τα εμφυτεύματα στήθους δεν πρέπει να θεωρούνται ως προέκταση του μπότοξ και της κοπής των φρυδιών σας.
Πρόκειται για σημαντικές χειρουργικές επεμβάσεις και μπορεί να υπάρξουν σοβαρά προβλήματα».
Πρόσθεσε ότι θα πρέπει να παρέχονται στον ασθενή εξέχουσες προειδοποιήσεις σχετικά με πιθανές παρενέργειες σύμφωνα με τις προειδοποιήσεις για το «μαύρο κουτί» που χρησιμοποιεί η FDA.

Η Suzanne Turner, καθηγήτρια κυτταρικής και μοριακής βιολογίας όγκων στο Πανεπιστήμιο του Cambridge, είπε ότι το εμφύτευμα με υφή Allergan Biocell που είχε συνδεθεί με υψηλότερα ποσοστά BIA-ALCL αποσύρθηκε οικειοθελώς από τον κατασκευαστή τον Ιούλιο του 2019.
Από τις 733 περιπτώσεις καρκίνου που εντοπίστηκαν από ο FDA τον Ιανουάριο του 2020, αναφέρθηκε ότι 620 αφορούσαν προϊόντα Allergan.
Ο Turner, ο οποίος διερευνά εάν το BIA-ALCL μπορεί να συνδέεται με χημικές ουσίες στα εμφυτεύματα, είπε ότι οι ρυθμιστικές αρχές θα πρέπει να εξετάσουν το ενδεχόμενο απόσυρσης άλλων εμφυτευμάτων στήθους με υφή.
Συγκεκριμένα ανέφερε τα εξής:
«Ίσως θα έπρεπε να καταλάβουμε περισσότερα για τη σχέση μεταξύ αυτών των εμφυτευμάτων και του καρκίνου προτού τα αφήσουμε να χρησιμοποιηθούν ελεύθερα», ενώ πρόσθεσε πως “οι ασθενείς που είχαν κάνει τα εμφυτεύματα αντιμετώπιζαν μικρό κίνδυνο και δεν τους συμβουλεύτηκε να τα αφαιρέσουν.
Θα πρέπει να επικοινωνήσουν με έναν γιατρό εάν παρατηρήσουν ξαφνική εμφάνιση πρηξίματος, εξόγκωμα ή/και πόνο”.
Η Nora Nugent, πλαστικός χειρουργός και μέλος του συμβουλίου της Βρετανικής Ένωσης Αισθητικών Πλαστικών Χειρουργών (Baaps), είπε ότι η MHRA συμβουλεύεται το ρυθμιστικό σύστημα για ιατρικές συσκευές, συμπεριλαμβανομένων των εμφυτευμάτων, κάτι που μπορεί να οδηγήσει σε νέες απαιτήσεις σχετικά με τις συμβουλές που δίνονται στους ασθενείς.
Συνιστάται ήδη στα μέλη του Baaps να συζητήσουν τον κίνδυνο του BIA-ALCL με τους ασθενείς.
Οι κανονισμοί για τα ιατροτεχνολογικά προϊόντα δεν απαιτούν επί του παρόντος να παρέχονται στους ασθενείς γραπτές προειδοποιήσεις για τις πιθανές αρνητικές επιπτώσεις των εμφυτευμάτων στήθους, αλλά οι κλινικοί γιατροί έχουν νομική υποχρέωση να συζητούν τους πιθανούς κινδύνους με τους ασθενείς.
Το MHRA είπε ότι η διαβούλευσή του πρότεινε μια νέα απαίτηση για παροχή πληροφοριών για τα εμφυτεύματα στους ασθενείς σε φυλλάδιο ή ψηφιακή μορφή.
Ένας εκπρόσωπος είπε: «Αυτό θα μπορούσε να περιλαμβάνει μια προειδοποίηση ότι ενδέχεται να προκύψουν κίνδυνοι κατά τη χρήση μιας εμφυτεύσιμης συσκευής».